近日,消化道微生物研究团队余凯凡副教授在Pharmacological Research期刊(IF:9.3)发表了题为“Succinate signaling attenuates high-fat diet-induced metabolic disturbance and intestinal barrier dysfunction”的研究论文,揭示了琥珀酸信号在高脂饮食引起的代谢紊乱和肠道屏障功能失调中的调节作用机制。

肠道屏障功能受损及其致使的肠道微生物和膳食成分易位被认为是肥胖发生的主要机制。饲喂高脂饮食(HFD)会引起微生物菌群失衡,进而损害黏液层屏障,泄漏的细菌及其产物(如脂多糖等)会进入循环和外周组织,最终加剧炎症和肥胖进程。琥珀酸是宿主细胞三羧酸循环的中间产物,同时也是肠道微生物发酵碳水化合物重要的代谢产物。由于在许多病理条件下(如抗生素性腹泻、炎性肠病等),血液及肠道中的琥珀酸水平异常升高,早前的一些研究将琥珀酸视为炎症标志物。然而,近年来,越来越多的研究指出琥珀酸具有广泛的代谢益处,包括激活肠道糖异生、促进脂肪产热、缓解肥胖引起的巨噬细胞炎症等。琥珀酸受体(SUCNR1)是一种G蛋白偶联受体,其参与介导琥珀酸的各种胞外信号作用。已有证据表明琥珀酸-SUCNR1信号参与小肠黏膜2型免疫的激活和肠上皮细胞的更新重塑。然而,琥珀酸-SUCNR1信号在肥胖相关的肠黏膜屏障损伤中的作用尚不清楚。
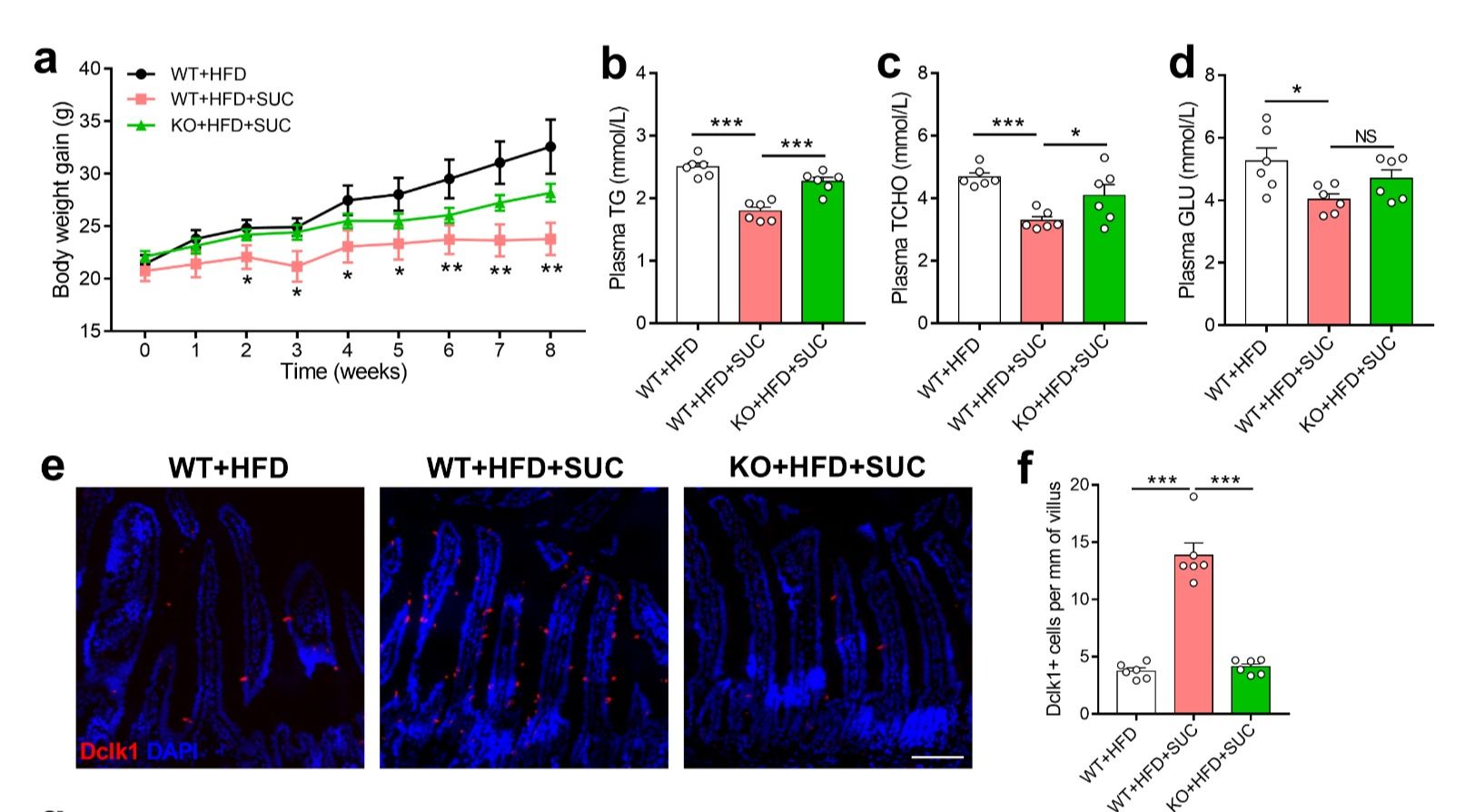
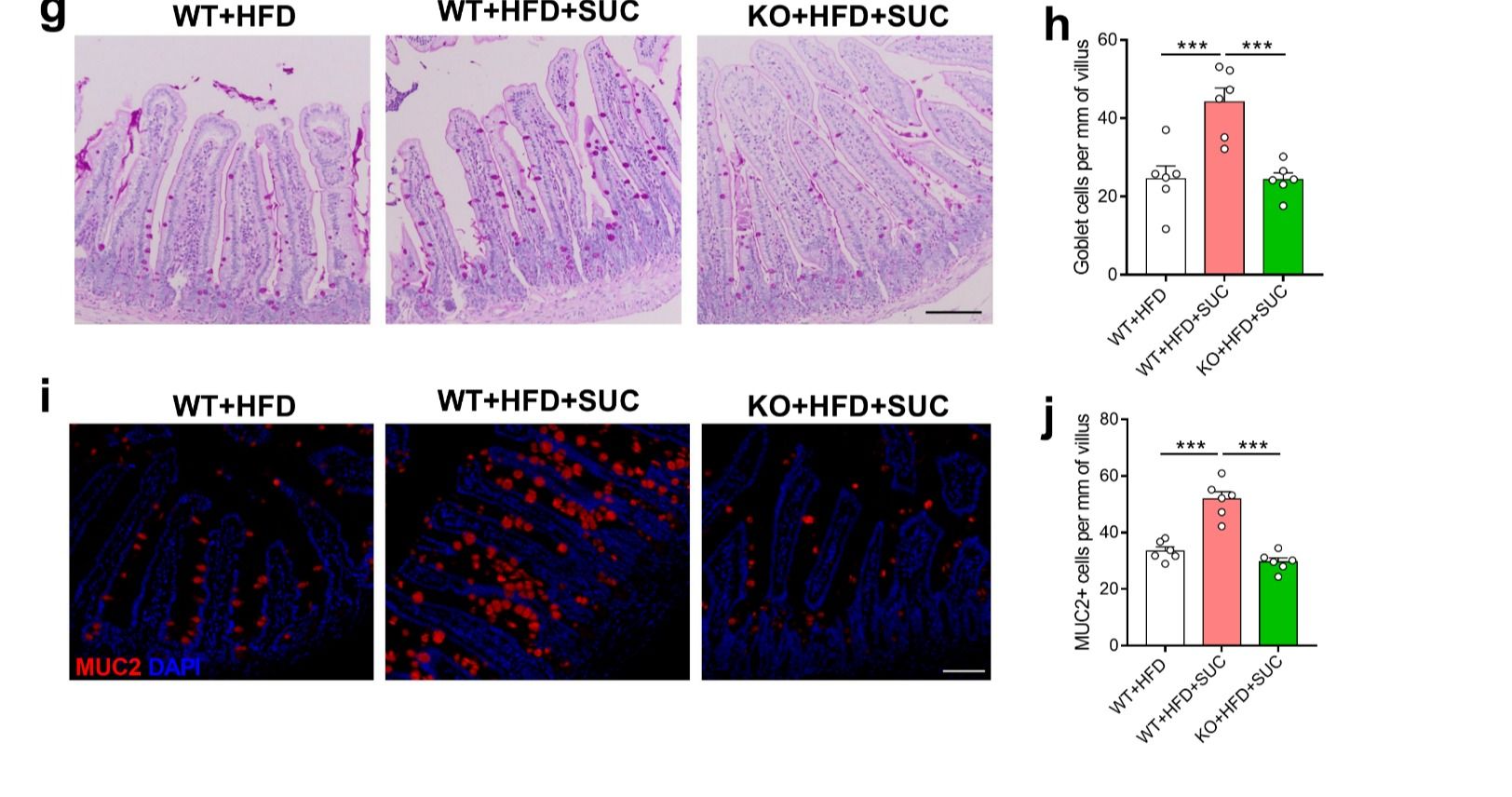
在本研究中,以6周龄大的SUCNR1敲出小鼠和同窝野生型小鼠作为动物模型,探究了琥珀酸信号在HFD诱导的肠黏膜屏障损伤中的作用。研究发现HFD饲喂显著减少了小肠杯状细胞的数量和黏液的产生,增加了肠道通透性,促进了肠道炎症。饮食补充琥珀酸能够激活小肠2型免疫,促进杯状细胞的产生和黏液的分泌,改善肠黏膜屏障完整性和微生物区系失衡,进而抵抗HFD诱导的体重增加,然而在SUCNR1敲出小鼠中这些改善作用消减。研究揭示琥珀酸对肠黏膜屏障的改善作用依赖于SUCNR1的表达。
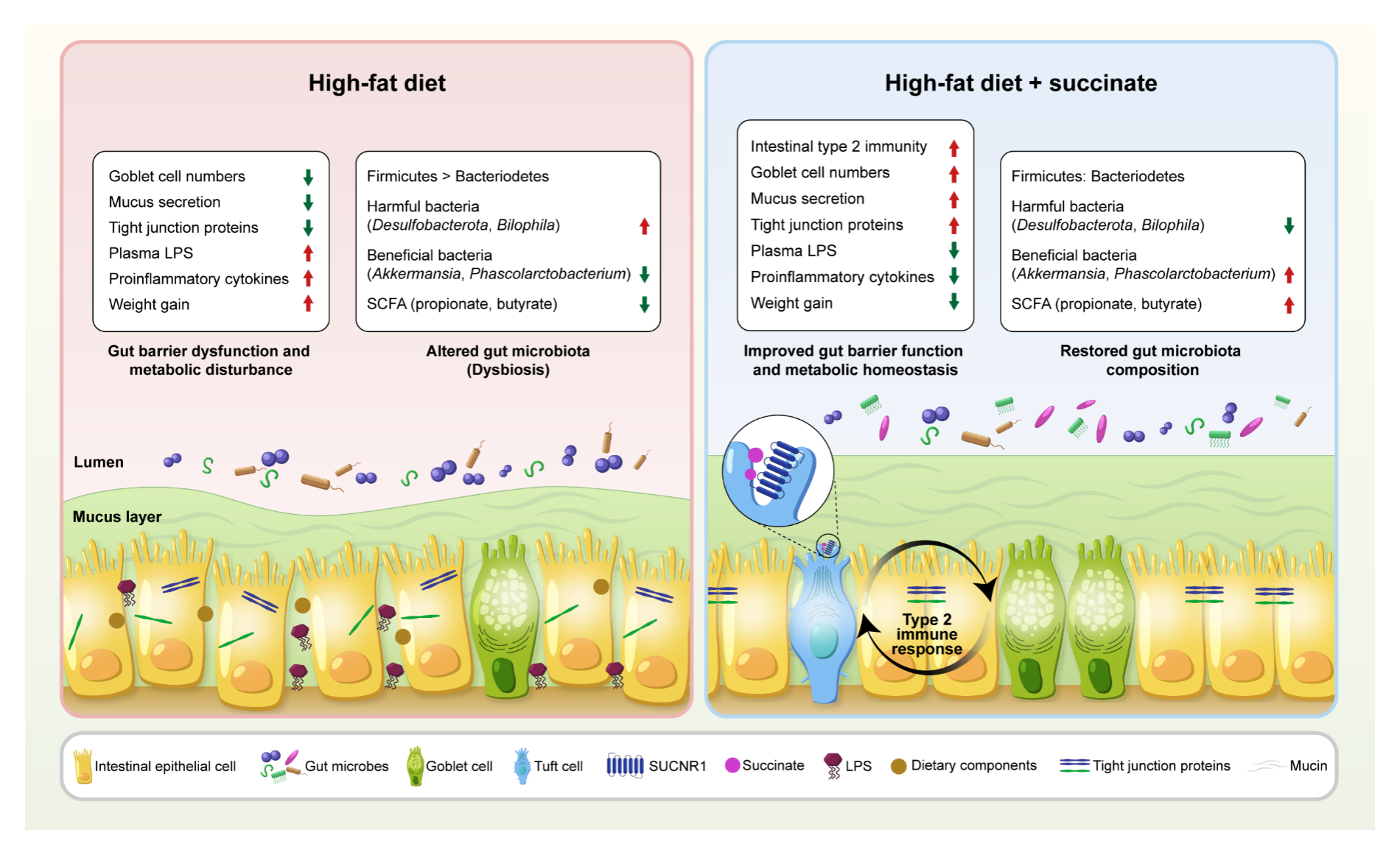
此研究表明,琥珀酸信号能够激活肠道2型免疫应答,驱动小肠杯状细胞的增殖分化和黏液的分泌,缓解高脂饮食诱导的肠黏膜屏障损伤和微生物区系失衡,最终发挥肥胖抵抗作用。这一发现强调了琥珀酸-SUCNR1信号对预防和治疗肥胖相关肠道疾病的重要性,为靶向琥珀酸-SUCNR1轴调控肠道健康提供了参考。
中心研究生李轩和黄国文为文章的共同第一作者,余凯凡副教授为通讯作者,中心主任朱伟云教授参与指导了该项研究。该研究得到国家自然科学基金项目(31972528)和江苏省农业科技自主创新项目(CX(19)3012)的资助。
原文链接:https://doi.org/10.1016/j.phrs.2023.10686